【福利贴:听白酒专场策略会,抽取茅台酒!】林园+但斌+5基金经理+6分析师(抽奖:茅台酒)
如果说2015年是中国药物创新的元年,刚刚过去的2020年,则是中国制药业创新成就最大的一年。
2020年,727件国产1类创新药临床申请获批准,较2019年增长114%;15个国产1类创新药获批上市,较2019年的9个增长67%。不过,与欧美等先进国家的差距仍在,急功近利的问题尚存,同质竞争的风险也已显现。从创新布局来看,快速跟进依然是大多数制药企业的主要做法,真正具有创新性且处于全球领先的产品占比还较少。
中国制药业交出历史上最靓丽的创新成绩单
证券时报创新医药部新药数据库显示,2020年药审中心受理国产1类创新药注册申请828件,其中受理临床申请781件,上市申请43件,与2019年相比,受理临床申请和上市申请数量分别增长了55%和72%。按药品类型统计,化学药574个,生物制品254个。
审评通过方面,2020年药审中心审评通过批准国产1类创新药临床申请727件,较2019年的340件增长114%。2020年国家药品监督管理局共批准15个国产1类创新药上市,较2019年的9个增长67%。
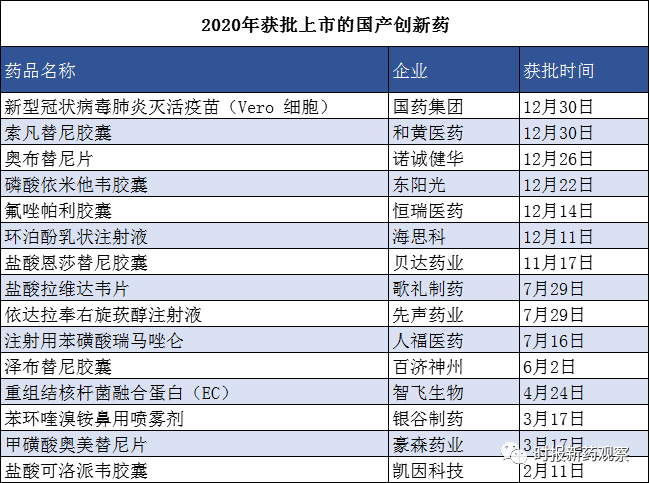
2020年8月4日,证券时报正式发布“人民金融·创新药指数”。截至12月31日,“人民金融·创新药指数”追踪的创新药升至701个,较7月1日基准日增加了179个成分样本,指数累计上涨32.55%。
在“人民金融·创新药指数”的成分样本中,目前有70%的品种进入了临床试验阶段,其中8个获批上市,32个处于上市申请阶段,21个处于三期临床或关键临床阶段,这些品种有望在未来数年内惠及患者。其中,泽璟制药的多纳非尼被称为2020年全球具有进程碑意义的临床研究,目前一线治疗晚期肝细胞癌III期研究达到了预设的主要终点,有望在2021下半年获批上市。
过去我国是单纯的新药引进国,而2020年一批中国本土公司自主研发的项目成功实现对外授权,既有获批上市的新药、临床阶段项目,也有一些临床前项目、创新前沿专利技术。如2020年6月9日,信达生物宣布与罗氏集团达成研发战略合作,涵盖多个肿瘤细胞治疗和双特异性抗体。2020年8月18日,又与礼来制药达成扩大免疫肿瘤药物抗PD-1单克隆抗体达伯舒®的战略合作,新的合作将拓展至全球市场。
2020年,对外授权的新药或在研项目交易总额在1亿元美金以上的中国药企就超过18家。如果说2006年石药集团向美国转让恩必普软胶囊专利使用权还是个例,如今中国药企对外授权已是多点开花,并呈现出多样性。
展望2021年,我国创新药审评审批有望取得更大的成就。在“人民金融·创新药指数”处于上市申请阶段的成分样本中,预计有19个有望在2021年获批上市。其中,艾力斯的甲磺酸伏美替尼、智飞生物的母牛分枝杆菌疫苗(结核感染人群用)等进展较快,有望在2021年1季度获批上市。
 上市药企和一批创新药研发企业成为创新主力
上市药企和一批创新药研发企业成为创新主力上市药企是我国新药创制的主力军,“人民金融·创新药指数”的701个成分样本,来自于91家上市药企(包括在国内、香港和美国上市的公司)和249家非上市药企的创新药。其中,91家上市药企贡献了357个,占比51%。以上市地点分,91家上市药企有61家是A股上市公司,20家是港股上市公司,7家是美股上市公司,3家是A+H股上市公司。
另一方面,非上市药企也展现出蓬勃的创新力,249家非上市药企拥有在研创新药,表明我国仍有大量创新性生物医药公司具有上市潜力。此前,不少小型生物技术药企定位于创新药,但受制于没有利润,故而未上市。近年的IPO改革为这类企业“敞开”了大门,2020年艾力斯、药明巨诺、德琪医药等多家未盈利的创新型药企成功登陆资本市场。
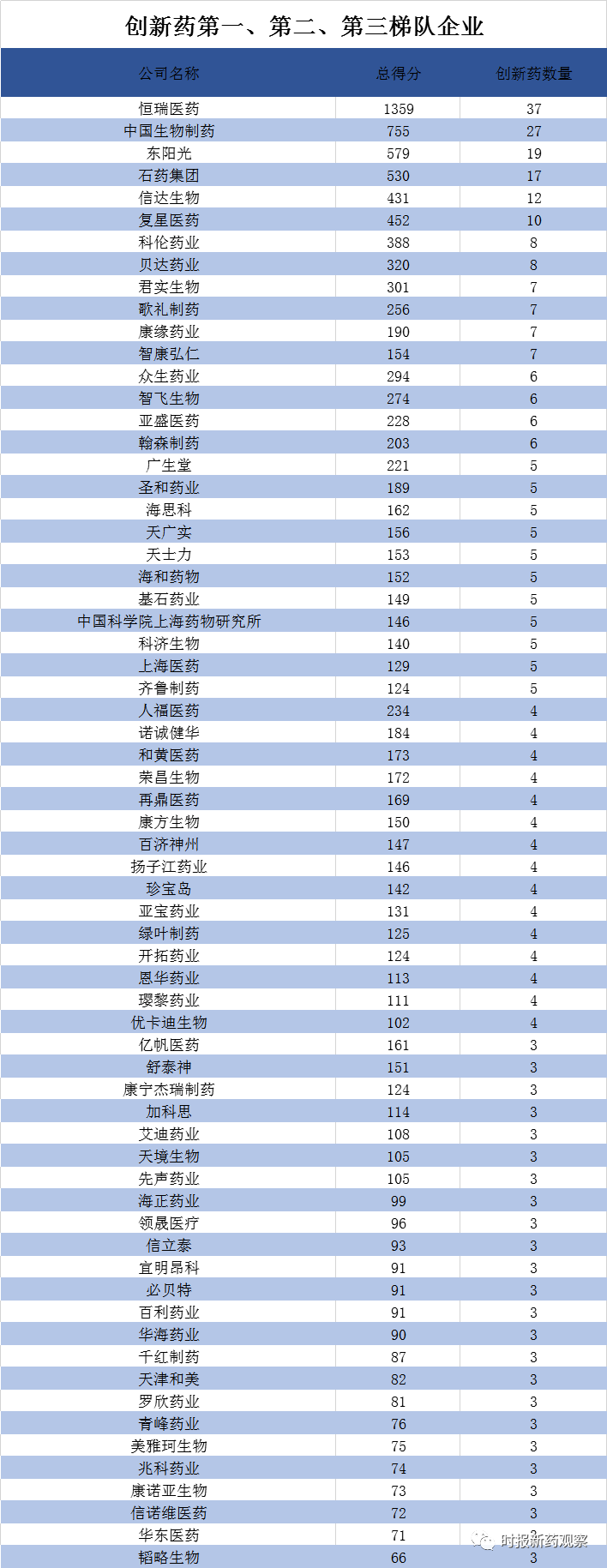
我国创新药研发呈现出马太效应,头部企业往往拥有多个或一批创新药品种。以数量计,创新药第一梯队有6家企业,分别是恒瑞医药、中国生物制药、东阳光、石药集团、信达生物和复星医药,这些企业均有10个以上创新药。
恒瑞医药表现最为突出,有37个创新药被纳入指数。从布局来看,抗肿瘤药是其布局核心,37个创新药中有半数是抗肿瘤药物。恒瑞医药坚定地执行快速跟进策略,紧随国际前沿热门靶点,且进度保持居于前列,其EZH2、CD47、c-Met、PD-L1/TGFβ等靶点药物国内最早进入临床。
其次是中国生物制药,有27个创新药被纳入指数,创新药得分为755,公司处于向创新药转型的关键时期,近5年累计研发费用近90亿元,5年复合增长率达23%。东阳光、石药集团、信达生物、复星医药也是公认的创新药龙头,创新药得分均超400分。
中国生物制药、东阳光、复星医药布局以化药为主,生物药布局较少,中国生物制药和复星医药过半创新药均属于抗肿瘤领域,也布局抗感染和消化系统药物;东阳光的创新药布局较分散,以抗感染药物和呼吸系统药物为主。
近年来,石药集团在研发上聚焦抗肿瘤领域,在其17个创新药中有11个属于抗肿瘤药,石药集团化药、生物药布局趋于全面,且生物药赛道布局超前,在其4个生物药中,既有全新靶点的单抗药物,又有热门的双抗和抗体偶联药物。信达生物是我国生物医药近年来发展的代表性生物技术公司,已有6款双抗获批开展临床试验,是国内双抗布局最广的企业。在信达生物的双抗品种中,同时靶向PD-1/PD-L1的IBI318进展最快,于2020年10月中旬登记启动了2期临床。
第二梯队包括科伦药业、贝达药业、康缘药业、君实生物等21家企业(含科研院所和大学),均有5个以上创新药,其中君实生物、亚盛医药、翰森制药、基石药业等是资本市场的新面孔,第二梯队多为研发布局以肿瘤靶向药物为主的生物科技企业。
第三梯队包括珍宝岛、天境生物、先声药业、璎黎药业等39家企业(含科研院所和大学),均有3个以上创新药。第三梯队中也不乏有重磅品种的企业,如2020年天境生物签署了其CD47单抗两项重磅合作,涉及金额超百亿元,创下中国生物制药企业向海外授权交易的新纪录。先声药业1类新药依达拉奉右莰醇注射用浓溶液2020年7月底获批上市,是近5年来全球唯一获批的脑卒中新药,该药在获批5个月后即进入医保,有望实现研发成果的快速变现。
第一、第二和第三梯队企业分别拥有122个、123个和129个创新药,合计占到创新药总数的53%。
从地区分布来看,第一、第二和第三梯队66家创新药企业集中分布在江苏和上海,两地分别有17家和14家企业,合计占到总数的近一半;其次是浙江和广东,均有7家创新药企业,其余企业主要分布在北京(5家)、四川(3家)、天津(2家)等省市。
资本市场、医保和药审制度改革形成了强大推动力
创新药研发周期长、投入大,国际上,一个创新药的研发周期在10年以上、投入在20亿元以上,没有强大的制度支撑,换不来如今我国药物创新的成就。
2020年,A股和港股生物制药IPO企业合计达到51家,较2019年大幅增长122%。资本市场改革一定程度上解决了创新药研发周期长、投入大的问题。
2018年的港交所改革、2019年的科创板落地,以及2020年创业板注册制的实施,向进入临床二期、尚未盈利的创新药企业“敞开”了大门,不仅解决了部分创新药企业的研发资金问题,也给创新药创业者带来了强劲的激励,给投资机构提供了高效的退出渠道,从而从更大层面上激励科学家和企业对创新药的投入。2020年全球生物医药领域融资事件中,晶泰科技、联拓生物、云顶新耀3家创新药企融资额均在3亿美元以上。
目前,在“人民金融·创新药指数”的创新药企业中,天广实、凯因科技、倍特药业、一力制药四家药企正在冲击IPO,2021年有望登陆A股市场。上海证券交易所科创板最新公示,凯因科技的上市申请已于近日注册生效。这意味着该公司有望于近期正式在科创板上市。根据招股说明书,凯因科技本次公开发行拟募资约10.92亿元,募集资金计划将主要用于新药研发。
2015年以来,国家药监局持续改革药品审评审批制度,完善药品研发、注册、生产监管,加快新药上市速度。2020年,新修订的《药品管理法》正式实施,国家药监局出台《药品生产监督管理办法》、《药品注册管理办法》《疫苗生产流通管理规定(征求意见稿)》等,完善上市许可持有人(MAH)主体责任及相关制度,最近又在上海、深圳等地设立了审评分中心,鼓励创新的氛围逐渐形成,大量符合条件的药物可通过突破性治疗药物、附条件批准、优先审评审批、特别审批四个加快通道获批上市。
国家医保局在2018年组建后整合了医保政策、基金管理、药品价格管理、招标采购等各项职能后,积极探索仿制药药品带量采购、国家药品价格谈判和医保目录调整,在约束仿制药盈利空间的同时,为创新药使用腾出了空间,推动药企加大创新药的研发投入。而新修改的《专利法》新增了关于药品专利最长5年补偿期的规定,也给新药研发带来重大利好。
此外,近年,除了国家层面外,江苏、上海、广东、北京等地纷纷出台政策支持苏州、张江、大兴等医药创新园,培育出了一批优秀的创新药企业。
在制度的感召下,越来越多的海外创新药人才归国,为创新药行业带来强大的技术支持。在政策、人才和资本的推动下,未来几年国产创新药有望迎来黄金发展期。
我国药物创新短板仍较为明显
2020年,FDA共批准53款新药(截至2020/12/25),其中包括39个新分子实体和14个新生物制品,远超我国批准的数量。从创新程度看,2020年FDA批准的新药中,有9款属于First-in-class药物(全球首创靶点或机制的创新药),而2020年我国获批上市的创新药多为快速跟进品种,表明我国药物创新要赶上欧美的步伐还有很长的一段路要走。
2020年底,火爆的PD-1市场迎来“寒冬”,在医保谈判中,三大国产PD-1单抗全部进入医保目录,但价格降幅空前。而据中信证券研报,近3年来,每季度申请PD-1的临床试验数量稳步增长,截至2020年三季度,共有314项进行中的PD-1/PD-L1临床试验,其中国内药企申办的占其中的209项。面对PD-1的定价,很难想象后来者还有多少利润可言。
PD-1药物扎堆是国内新药研发同质化的一个缩影。从创新布局来看,我国有超过一半在研创新药的适应症集中在抗肿瘤,绝大部分的创新都是针对国际热门靶点进行的快速跟随,且基于同一靶点的研发同质化程度高;另外,针对新靶点设计的完全创新的新药数量也较少,这是我国创新药研发暴露出的短板。
创新药研发同质化带来的是被市场淘汰的风险将增加,最终可能挫伤研发的积极性,造成资本和人力的浪费。因此,国内做创新药研发的企业应对此保持警醒,选择具有中国特色的赛道进行差异化创新,如孤儿药、罕见病药等或更有前途。另外,药物创新要站在技术前沿,避免技术迭代加快带来的挤出效应。在创新药逐步向差异化、国际化发展之时,创新药行业也会迎来高质量的发展,最终开发真正的全球首创新药。
近日,《医药魔方》刊发了一篇《中国first in class新药研发,还缺什么?》的文章。文章说,国内在研品种中也不乏全新靶点或机制的药物,但绝大多数并未进入临床,或是进入临床不久后即停滞不前,问题的核心是转化研究不足。
创新药研发通常可以划分为三块:基础科研、转化研究和临床研究,基础研究和临床研究之间往往上存在较大的间隔,而桥接两者的,是转化研究。基础科研方面,近十余年中国已取得长足进步;临床研究方面,中国临床研究有诸多明显优势;相较而言,中国的转化研究明显偏弱,这背后的原因包括基础和临床的长年割裂、行业观念和认可度的不足、领导者和执行团队的欠缺等诸多历史因素,虽然近年来也开始有所改善,但仍然距离国际领先水平有较大差距。
近几年,IPO制度的改革为众多创新药企业提供了上市机遇,医药企业成为了IPO的主力军。但另一方面,创新药企业“破发潮”也悄然来临,已有相当大一批未盈利生物医药公司股价已跌破发行价,或者逼近发行价。截至2020年底,在2020年上市的未盈利的创新药企业中,百奥泰、和铂医药、德琪医药、嘉和生物、开拓药业等跌破发行价,若是将时间线放的更长,则还有迈博药业、基石药业、东曜药业、中国抗体、复宏汉霖等股价也已位于发行价下方。
究其原因,或是资本市场从初期的对创新药一味地追棒进入了冷静期。经过时间的沉淀,最终研发管线优异和商业化能力强的创新药才会被市场认同。从这个角度来看,创新药企只有搞真正的创新药研发、走差异化道路才会胜出。证券时报医药部时报新药观察
扫二维码 领开户福利!
郑重声明:本文版权归原作者所有,转载文章仅为传播更多信息之目的,如作者信息标记有误,请第一时间联系我们修改或删除,多谢。



